Fetal medicine
Imagerie
Publié le 29 Apr 2025Lecture 5 min
L’œsophage fœtal et ses anomalies en échographie
Jean-Philippe BAULT, Plateforme Lumière Necker, CPDP CHI Poissy–Saint-Germain, Cabinet d’échographies gynéco-obstétricales, Les Mureaux
Les récentes recommandations de la CNEOF d’octobre 2023 n’incitent pas à visualiser l’œsophage fœtal dans le cadre du dépistage. Seules les recommandations du Comité national technique de l’échographie de dépistage prénatal de mars 2010 concernant l’échographie de diagnostic mentionnent de rechercher la continuité œsophagienne dans le cas où l’estomac serait petit ou absent(1).
Il est néanmoins beaucoup plus facile aujourd’hui, grâce aux progrès techniques considérables du matériel échographique, de mettre en évidence cet organe qui est, de façon non exceptionnelle, le siège de pathologies devant être prises en charge dès la naissance.
Visualisation échographique de l’œsophage
La difficulté de visualisation de l’œsophage est liée à plusieurs facteurs : d’une part, sa position profonde dans le médiastin avec interposition de structures antérieures (en particulier les clavicules) qui créent des cônes d’ombre, et, d’autre part, son trajet initialement parfaitement sagittal devenant oblique vers la gauche dans sa partie inférieure.
Le plan de coupe idéal est donc sagittal avec une discrète obliquité vers la gauche au niveau de la coupole diaphragmatique (figure 1).
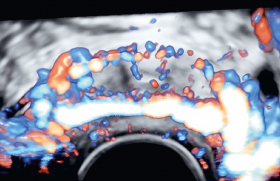
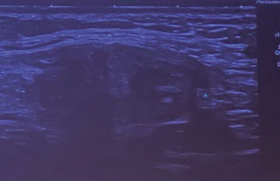
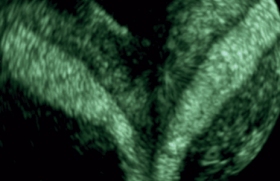
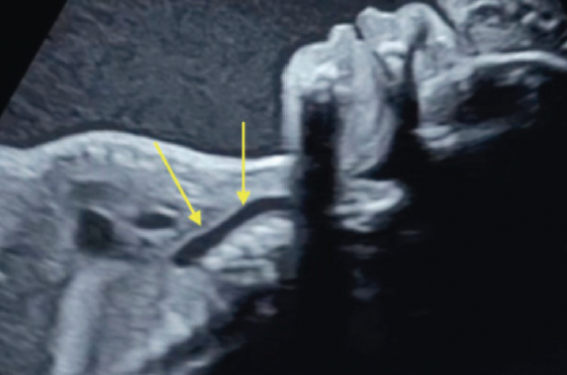
L’œsophage apparaît comme une structure échogène feuilletée (5 feuillets) située en avant du rachis et de l’aorte, et dans sa partie supérieure en arrière de la trachée (figure 2). Un épisode de déglutition peut faciliter la mise en évidence de sa continuité (figure 3).
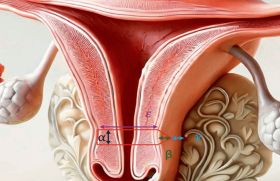
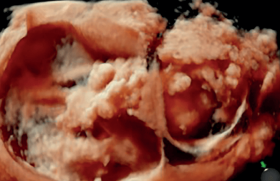
Le plan frontal peut aider à visualiser sa partie inférieure (figure 4).
Il est à noter qu’il est particulièrement facile de mettre en évidence l’œsophage au 1er trimestre en raison de son aspect très échogène (figure 5).
Figure 1. Plan de coupe permettant de visualiser l’œsophage.
Figure 2. OEsophage (flèches jaunes), trachée (flèches vertes).
Figure 3. OEsophage lors d’un épisode de déglutition (flèches jaune).
Figure 4. OEsophage plan frontal. A : aspect feuilleté. B : en cours de déglutition.
Figure 5. OEsophage au 1er trimestre.
Pathologies de l’œsophage
Atrésies
La principale pathologie est l’atrésie. Sa fréquence est estimée entre 1/2500 et 1/3800 naissances vivantes(2,3). C’est l’une des pathologies fœtales les plus souvent méconnues. Elle n’est isolée que dans 50 % des cas.
Cinq types différents sont distingués (figure 6), seule la forme « A » n’est pas associée à une fistule œsotrachéale. La forme « C » médiastinale avec fistule entre la trachée et la partie inférieure de l’œsophage est la plus fréquente (88 %).
Les signes d’appel sont l’association d’un hydramnios et d’un estomac absent ou franchement petit. Parfois, des vomissements peuvent être mis en évidence grâce à l’utilisation du Doppler avec PRF basse.
Les signes diagnostics :
– le signe de la poche (pouch sign) essentiellement cervicale est pathognomonique. Ce signe est d’autant plus difficile à mettre en évidence que le terme est précoce ; les mouvements de déglutition étant peu fréquents dans cette période de la grossesse (figure 7) ;
– la non-visualisation de l’œsophage dans l’espace interaorto-trachéal (figure 8) ;
– l’empreinte trachéale.
L’œsophage et la trachée ont la même origine embryologique : l’intestin antérieur. En cas d’atrésie de l’œsophage, la trachée présente une trachéomalacie et vient donc combler le défect œsophagien (figure 9) ;
– parfois, il est possible dans les atrésies de type C de mettre en évidence la fistule (figure 10).
Figure 6. Types d’atrésies de l’œsophage.
Figure 7. Atrésies de l’œsophage : Pouch sign.
Figure 8. Atrésie de l’œsophage. A : absence de l’œsophage dans l’espace inter-aorto-trachéal. B : témoin normal (images J.E Morice).
Figure 9. Empreinte trachéale.
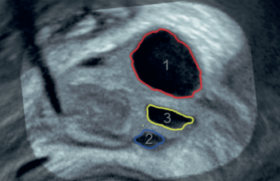
Figure 10. Atrésie avec fistule : trachée (flèche jaune), œsophage (flèche rouge) fistule (flèches bleues).
Dans la série publiée en 2021 par Kassif et coll.(2), il apparaît clairement que le type A (sans fistule) est le plus facile à diagnostiquer (100 % de diagnostics positifs), d’autant que ce type est toujours associé à des signes indirects : polyhydramnios et estomac petit ou absent.
La série réalisée à Necker(3) attribue aux ultrasons isolés seulement 41 % de sensibilité. L’appel à d’autres moyens diagnostics, en particulier dans les atrésies de type C est donc indispensable pour améliorer la sensibilité du diagnostic :
– le dosage des enzymes digestives (GGTP gamma glutamyl transpeptidase et AFP Alpha fœto protéine avec un index > 3) présentant ainsi une sensibilité de 89,9 % ;
– l’IRM, réalisée après suspicion par les ultrasons, ayant quant à elle une sensibilité de 94,7 %.
La mise en évidence d’une atrésie impose la réalisation d’un bilan – caryotype et ACPA, échographie de référence – à la recherche :
– d’un RCIU, présent dans près de 40 % des cas ;
– des signes évocateurs d’une association VACTERL (figure 11) retrouvés dans plus de 50 % des cas(1).
Notons que la découverte d’un ou a fortiori de plusieurs signes pouvant entrer dans le cadre d’une association VACTERL doit impérativement faire rechercher une atrésie œsophagienne avec fistule.
Néanmoins, quelle que soit la qualité de l’expertise, un certain nombre de cas sont méconnus ou suspectés à tort. La répétition des examens, l’appel aux autres moyens diagnostics préalablement évoqués doivent permettre d’améliorer le taux de diagnostics positifs.
Figure 11. Association VACTERL (signes).
Duplications
Elles sont extrêmement rares, non syndromiques. Elles peuvent être soupçonnées devant la découverte en anténatal d’une image de dédoublement de la partie inférieure de l’œsophage sur une coupe axiale (figure 12).
Figure 12. Duplication de l’œsophage : œsophage dilaté(*), duplication (flèches turquoises), aorte (flèches bleues).
Mégaœsophage
Il pourra exceptionnellement être évoqué devant la présence d’un œsophage dilaté dans sa partie inférieure, et ce de façon quasi permanente (figure 13).
Figure 13. Mégaœsophage.
La mise en évidence de l’œsophage est donc un défi qui nécessite une connaissance précise de l’anatomie fœtale, une excellente expertise. L’étude systématique, l’amélioration des techniques échographiques et la patience de l’opérateur devraient permettre d’améliorer la mise en évidence de l’œsophage et de ses anomalies dans l’avenir.
1. Lansac J, L’échographie de diagnostic, Rapport du CNTEDP, mars 2010.
2. Kassif E, Weissbach T, Kushnir A et al. Esophageal atresia and tracheoesophageal fistula: prenatal sonographic manifestation from early to late pregnancy. Ultrasound Obstet Gynecol 2021 ; 58 : 92-8.
3. Spaggiari E, Faure G, Rousseau V et al. Per formance of prenatal diagnosis in esophageal atresia. Prenat Diagn 2015 ; 35 : 888-93.
4. Bault JP, Levaillant JM, Couly G, Heurteloup E, Atlas d’écho-anatomie foetale, Sauramps éditeurs, 2021.
5. Bault JP, Levaillant JM. Échographie obstétricale dépistage et diagnostic; Tome 2 : Morphologie normale du foetus
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :